
弹道碎石术依赖于弹丸运动产生的能量。弹丸的初始运动可以由各种刺激引起,柔性物体可以保持能量的动量,但是相对固定的物体,比如结石,碎石时的碎片,一旦弹丸与另一物体接触,弹道能量就转移到物体上(“手提钻”效应)。
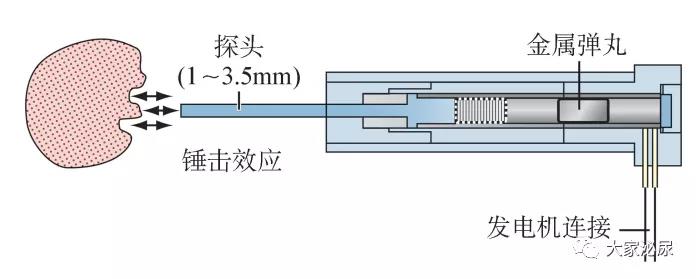
图1:手持式碎石器
1.弹道碎石术发展进程
20世纪90年代初,瑞士LithoClast是第一个弹道式碎石机。Rane和同事(2008)首次报道了一种新型手持式弹道碎石机Stone-Breaker(CookMedical,Bloomington,IN),这款便携式设备采用小型气缸式供气系统,而不是医院空气系统,简化了人体工程学配置。Wang和同事(2012)研究了另一种手持设备———瑞士LithoBreaker的一种电动装置。体外研究中发现,虽然它在输尿管镜下模型中有效,但在PNL模型中表现较差。
2.弹道碎石术优缺点
(1)优点
弹道碎石术可用于泌尿系所有结石,碎石效率高且安全性好。弹道碎石治疗各种成分的输尿管结石,碎石成功率在73%~100%,与EHL成功率相似。
弹道碎石的优势可能是治疗PNL术中大而坚硬的结石或膀胱结石。相比于输尿管结石,肾结石在弹道碎石过程中更容易被“固定”在尿道上皮上,从而比超声碎石更快,效率更高。当大块结石碎裂后,可结合超声碎石将细小的碎石吸出。相比EHL、超声碎石和激光碎石,弹道碎石引起的输尿管穿孔风险较小。由于弹道碎石不产热,因此不会引起尿路上皮的热损伤。
弹道碎石的另一优势是费用相对便宜,维护成本低。尽管该设备相比EHL贵,但是弹道碎石没有一次性耗材的损耗,且碎石杆的使用寿命相对较长。
(2)缺点
弹道碎石的缺点在于碎石杆不能弯曲,因此只适用于直工作通道的输尿管镜或肾镜。
此外,弹道碎石在碎石过程中可造成结石回缩。在治疗输尿管结石时,结石回缩率为2%~17%。通常碎石失败与无法在扩张的输尿管中有效的击碎结石相关。碎石造成的结石位移与结石位置相关,上段结石较下段结石在碎石过程中更容易位移。对于一些吸引装置如LithoVac吸引杆(Boston Scientific)是否可减少碎石时结石的位移,目前数据还较少。
利用弹道碎石将结石破碎至小于4 mm的碎片十分困难,特别是对位于扩张的输尿管中的质地较硬的结石。碎片大于4 mm,需要二期输尿管镜取石率较高。因此,在一期处理结石时应使用网篮或取石钳尽可能地将结石取出。
3.弹道碎石术技术要点
和其他碎石方法一样,气压弹道碎石需保持镜下视野清晰。与肾结石或膀胱结石不同,由于输尿管结石碎石有时难以固定结石,需要使用网篮将固定结石,或者使用输尿管封堵器。输尿管结石行弹道碎石的最终目的为将结石击碎为小于2 mm的碎片使其可自行排出。
弹道碎石引起输尿管损伤的风险较少,因此术后可不留置输尿管支架。Tan和其同事(1998)报道68例行输尿管镜弹道碎石,只有9例术后留置了输尿管支架。这些留置了输尿管支架的病例包括输尿管条件较差导致上镜困难或结石嵌顿部位有严重的血肿与损伤。
本文引自《坎贝尔-沃尔什泌尿外科学》第11版中文编译版